-
题目: 未知类型
某废水处理厂处理废水中NH+的过程如下: ①NH4+(aq)+
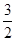 O2(g)=HNO2(aq)+H+(aq)+H2O(1) ΔH="-b" KJ/mol
O2(g)=HNO2(aq)+H+(aq)+H2O(1) ΔH="-b" KJ/mol②2HNO2(aq)+O2(g)=2NO3-(aq)+2H+ ΔH=-aKJ/mol
下列叙述正确的是( )
A.将NH4+转化为NO3-的热化学方程式可表示为: NH4+(aq)+2O2(g)=NO3-(aq)+2H+(aq)+H2O(1)ΔH=-(b+
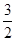 )KJ/mol
)KJ/molB.在上述两次转化过程中,废水的酸性先增大然后逐渐减弱 C.常温下,若HNO3溶液中c(H+)="0.1" mol·L-1,则该溶液的pH>1 D.若上述两次转化完全,不考虑其它杂质离子的存在,则:c(NH4+)+c(OH-)=c(NO3-)+c(H+) 答案不对?请尝试站内搜索
推荐知识点:
- 试析杜甫的儒家思想。
- 调度规程制定的依据是()、《电网调度管理条例》、《电力监管条例》和国家、地方政府以及上级电力管理有关部门制定的适用于电力工业的法律、法规及标准。
- 下列诗句中,运用了互文见义手法的是()
- 甲厂和乙厂都需要柴油,两厂与丙燃料公司订立了一份合同,约定丙燃料公司在1个月内供给0号或10号柴油1000吨,每吨价格为1600元。在柴油运到后,甲厂与乙厂按4比6分配,则该合同之债不属于()。
- 男,35岁。骑摩托车时摔倒,当时感左膝关节疼痛,活动受限,左小腿外侧感觉减弱,足不能背伸,足背动脉可触及,X线片示左膝关节胫骨向前,股骨下端向后。经上述处理后,神经损伤无修复,应进行下列哪项处理?()
- 顾客在消费活动过程中自始至终伴随着思维,这种消费思维通常有三个过程,即认识分析过程、比较择优过程和()。
- 诺兰将信息技术发展划分为几个时代,它们是()。
- 跨度在40M及以上的钢梁,由工务段负责至少每()年测量一次挠度和拱度。
- 鼻烟窝的解剖中,鼻烟窝的形状为()。
- 简答油气回收系统的日常检查内容。